Chimica 3.C 2025-26
(12.5.2026) - pg. 320, 321, 322
Le soluzioni acido - basiche
Soluzioni acquose
- molecolari
- ioniche
- acide
- basiche
- ioniche/saline
acido cloridrico HCI - ambientato nello stomaco e importante nell'industria
acido solforico H2SO4 - issatoin molti ambiti. Non si puè comprare in concentrazione di 15%
acido citrico C6H8O7 - E numero E330
acido formico CH2O2 - l'acido COOH più semplice
acido bromidrico HBr - Viene normalmente venduto in soluzione acquosa al 48%.
acido acetico (octová) CH3COOH -
acido buttirico -
acido benzoico -
acido triossocarbonico H2CO3 - nelle pioggie acide
acido lattico (kyselina mléčná) -
acido solforico H2S -
acido nitrico HNO3 -
Caratteristiche degli acidi e basi
acidi:
- sapore aspro
- capacità di sciogliere alcuni metalli
- capacità di fare cambiare il colore a certi estratti vegetali (tè diventa più trasparente se mettiamo un po' di limone)
- capacità di neutrilizzare i basi
Basi:
- sapore amaro
- consistenza viscida/lisciviosa (klouzavá) al tatto
- la capacità di ripristinare il colore originario degli estratti vegetali trattati con acidi
- la capacità di neutralizzare gli acidi
Neutralizzazione
- sali si formono dopo la reazione
Classificazzione degli acidi
-
inorganici (es. H2SO4, HNO3, HCl)
-
organici (es. acido formico, acido acetico, acido citrico)
-
forti (H2SO4, HNO3)
-
deboli (HCO3, HPO3, tutti gli acidi organici)
-
monovalenti/monoprotico (jednosytné) (HNO3, HCl, HMnO3) - un solo idrogeno
-
polivalenti/poliprotico (vícesytné) (H2SO4, H3PO4, H4SiO4) multipli idrogeni
Teoria di Arrhenius
acido è una sostanza che in soluzione acquosa libare uno o più ioni H+. Base è una sostanza che libera nelle soluzioni acquose CH-
13.5.2026 - pg. 322, 323
L'elletrolita: sostanze che in soluzione acquosa si scindono in ioni positivi e negativi jn grado di condurre la corrente elettrica; sino elettroliti gli acidi, le basi e i sali
- forti - sino completamente scissi (es. soluzione di NaCl --> Na+ + Cl-)
- deboli - scissi inioni solo parzialmente
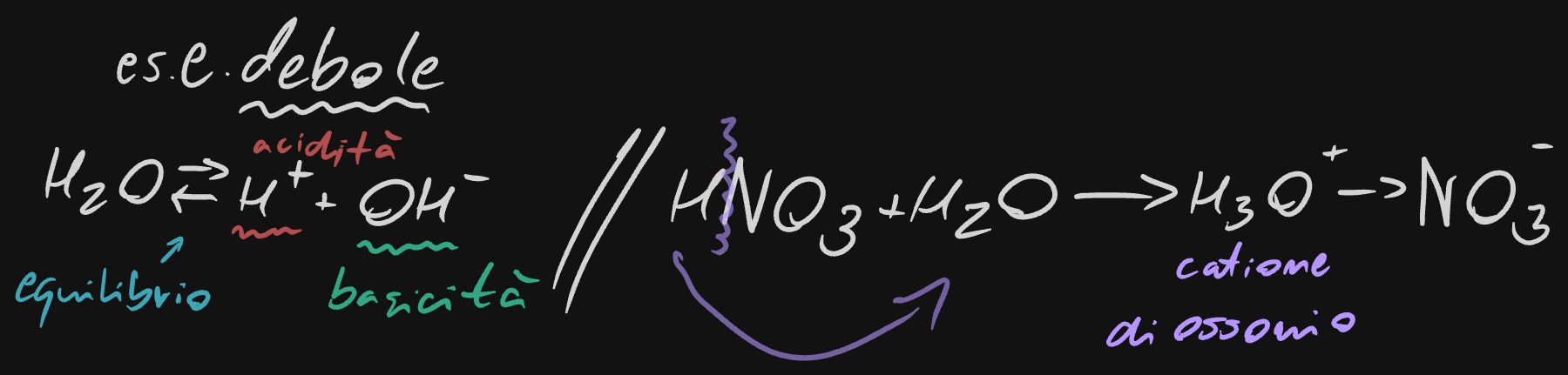
esempio di una scissione debole con un'altra versione
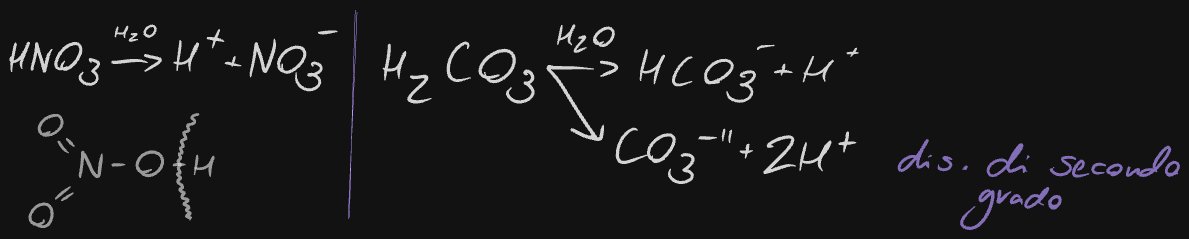
esempi delle scissioni - le scissioni di 2º grado sono più prevalenti
Teoria di Brönsted-Lowry
- non è limitata solo alle soluzioni acquose, ma anche per le soluzioni non-acquose